I basket e gli umbrella trial come nuova risorsa nella medicina di precisione
A cura di Martina Tammaro1
1Scuola di Specializzazione in Farmacia Ospedaliera – Università degli Studi di Milano ASST Spedali Civili di Brescia
Abstract:
Lo sviluppo delle tecnologie e delle banche dati biologiche ha portato alla differenziazione delle patologie neoplastiche in base alle mutazioni e all’utilizzo delle informazioni derivanti dal patrimonio genetico per sviluppare targeted therapies. Questo nuovo approccio terapeutico alla base della medicina di precisione ha portato allo sviluppo di nuovi disegni di studi clinici biomarker-guided: i basket trials e gli umbrella trials.Nei basket trials, uno stesso trattamento viene studiato per diverse patologie che presentano le stesse alterazioni molecolari, mentre negli umbrella trials molte targeted therapies sono sperimentate su una singola malattia stratificata in molteplici sottogruppi suddivisi per alterazioni genetiche. Nel 2018, l’FDA (Food and Drug Administration) sottolinea l’importanza di questi protocolli per migliorare l’efficienza delle cure e ne raccomanda l’utilizzo.
Questi trials rientrano nella medicina di precisione dove anche il farmacista può ricoprire un ruolo centrale nella ricerca, nell’interpretazione del sequenziamento genomico, nelle raccomandazioni da seguire relative al trattamento e nel facilitare l’approvvigionamento di farmaci off-label. Per questo nel 2014 l’Indiana University Health Simon Cancer Center ha iniziato un programma per implementare la medicina di precisione nella pratica clinica con un team multidisciplinare, dove anche il farmacista aveva un ruolo di leadership.
Last update: 14/12/2021
Introduzione
Nel maggio 2018 il National Institute of Health ha lanciato l’iniziativa ‘All of us’ il cui scopo è raccogliere i dati demografici e biologici di almeno un milione di persone per sviluppare trattamenti di precisione in oncologia e per differenziare le patologie in base alle mutazioni, in modo da scegliere le terapie in base a precisi biomarcatori [1]. La medicina di precisione è una forma di medicina che utilizza le informazioni sui geni o le proteine di una persona per prevenire, diagnosticare o curare la malattia. Nello specifico in oncologia utilizza informazioni specifiche sul tumore di una persona per aiutare a fare una diagnosi, pianificare il trattamento, scoprire come funziona il trattamento o fare una prognosi [2].
Il miglioramento della tecnologia e lo sviluppo della genomica, della proteomica e delle biopsie liquide, hanno permesso di utilizzare le informazioni derivanti dal sequenziamento genomico nella pratica clinica determinando specifici bersagli molecolari su cui scegliere una targeted therapy diventando uno standard of care oncologico nell’ottica della medicina di precisione [3]. La scoperta delle mutazioni somatiche ha rivoluzionato i trattamenti di molte patologie come la leucemia mieloide cronica e il carcinoma polmonare non a piccole cellule [4].
Questo nuovo approccio in oncologia che integra le analisi molecolari ai criteri clinico-patologici ha portato al superamento dei classici disegni degli studi controllati ed allo sviluppo dei biomarker-guided clinical trials e tra cui i basket e umbrella trials nella struttura del protocollo principale (o master protocol). [1, 5] Il master protocol è ideato per valutare molteplici ipotesi con l’obiettivo di migliorare l’efficienza e stabilire uniformità attraverso procedure standardizzate nello sviluppo e nella valutazione di diversi interventi. Può essere differenziato in molteplici studi subparalleli per includere trials standardizzati operazionali, strutture, reclutamento, selezione dei pazienti, raccolta e analisi dei dati [5]. Nei basket trial, una targeted therapy viene studiata per molte malattie che condividono le stesse alterazioni molecolari, senza tener conto della localizzazione anatomica della massa tumorale e dell’istopatologia quando viene assegnato il trattamento, mentre negli umbrella trials molte targeted therapy sono sperimentate su una singola malattia stratificata in molteplici sottogruppi suddivisi per alterazione genetica [1-5].
Nel 2018 la FDA ha rilasciato un documento che sottolinea le raccomandazioni per i basket e gli umbrella trials sottolineando l’importanza della diffusione di questi protocolli per migliorare l’efficienza delle sperimentazioni [6].
Nei basket trials i pazienti hanno criteri di eleggibilità unificati basati su fattori di rischio predittivi riferiti al meccanismo d’azione. Negli umbrella trials una singola malattia è stratificata in più sottogruppi con eleggibilità per ciascun braccio d’intervento definite dal meccanismo d’azione e ogni sottogruppo ha un biomarker diverso per valutare l’utilità di differenti targeted therapies.
Sia nel basket che nell’umbrella trial è presente un protocollo di screening comune per determinare l’eleggibilità dei pazienti. La maggioranza dei trials condotti sono di tipo oncologico nei quali è presente un protocollo di screening molecolare con dosaggi di biomarkers standardizzati.
In entrambe le tipologie di studi si possono avere uno o più gruppi di controllo (Figura 1 e 2). Per gli umbrella trials il gruppo di controllo può essere il placebo o, se esiste, il trattamento standard per quella patologia, che viene usato per tutti i sottogruppi; Nei basket trials la determinazione dei gruppi di controllo è più difficile perché vengono studiate più patologie: può essere placebo se non ci sono terapie di riferimento; se invece le terapie alternative sono diverse, è possibile che vengano somministrati differenti standard of care nel gruppo di controllo comune.
(a) Basket trial- no control group
(b) Basket trial-with control

|
Figura 1: esempio di un basket trial: (a) un basket trial a singolo braccio senza gruppo di controllo, (b) un basket trial randomizzato a due bracci [1]. |
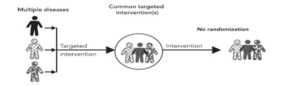
(a) Umbrella trial-no controls

(b) Umbrella trial-with controls

|
Figura 2: esempio di un umbrella trial: (a) umbrella trial non randomizzato con 3 interventi mirati, (b) un umbrella trial randomizzato che include 3 sottogruppi, ognuno con un intervento mirato e un controllo [1]. |
Questi trials hanno un approccio genomico e usano tecnologie sia per definire patologie e criteri di eleggibilità sia per migliorare la caratterizzazione e l’identificazione di biomarcatori predittivi. Inoltre, è importante l’uso di un singolo protocollo master con procedure standardizzate condivise tra i vari enti. Alcuni esempi rilevanti di basket trial che hanno portato all’approvazione nuovi farmaci o farmaci già esistenti ma per nuove indicazioni sono i seguenti: Entrectinib, che grazie al basket trial STARTRK-2 [7], è stato il terzo farmaco per curare i tumori su base genetica e molecolare a ricevere una procedura accelerata da parte di FDA; Vemurafenib per la malattia di Erdheim-Chester, raro tumore del sangue, è stato approvato grazie lo studio VE-BASKET [8]; altro esempio è l’approvazione di Pembrolizumab per i pazienti con tumori carenti di riparazione del mismatch (dMMR), indipendentemente dall’origine del cancro. [9] Per quanto riguarda gli umbrella trial, ad oggi nessuna di queste tipologie di sperimentazioni ha portato ad approvazioni di farmaci [1], ma sono in corso alcuni importanti studi riguardanti sia il tumore al polmone, come lung-MAP [10] e ALCHEMIST [11], sia il carcinoma del colon-retto, come il FOCUS4 [12].
Tali tipologie di studi presentano una serie di criticità come la plausibilità biologica delle strategie di intervento mirate, l’accuratezza dei saggi dei biomarcatori, la collezione di campioni biologici, la prevalenza dei biomarcatori e la randomizzazione con i fattori predittivi [1].
Il possibile ruolo del farmacista nella medicina di precisione
All’interno della medicina di precisione anche il farmacista potrebbe ricoprire un ruolo di rilievo e per questo l’Indiana University Health Simon Cancer Center ha implementato il ruolo del farmacista che lavora in ambito oncologico ed ematologico creando una medicina di precisione basata su un approccio definito “molecular tumor board”. Secondo questo approccio clinico innovativo viene costituito un team multidisciplinare formato da clinici e scienziati (fisici, genetisti e bioinformatici), che valuta il livello molecolare del tumore per erogare al paziente una targeted therapy specifica.
Solamente pochi programmi negli Stati Uniti hanno una forte presenza del farmacista onco-ematologico. Il farmacista in questi programmi riveste un ruolo di leadership nella ricerca, nell’interpretazione del sequenziamento genomico, nelle raccomandazioni da seguire relative al trattamento e nel facilitare l’approvvigionamento di farmaci off-label.
L’iniziativa della medicina di precisione nell’Università dell’Indiana fu stabilita dal presidente Barack Obama con un grosso investimento economico per identificare le mutazioni genetiche coinvolte nel cancro e per sviluppare approcci più efficaci da utilizzare nel trattamento della malattia. Il programma iniziò nel 2014 con un gruppo composto da oncologi, scienziati esperti in genetica molecolare, medici ricercatori e un farmacista esperto in oncologia; ora vengono inclusi anche coordinatori infermieristici, consulenti genomici, un data manager, un ricercatore oncologo e due farmacisti PGY-2 clinici oncologici. Da quando è iniziato il programma si sono sequenziati più di 1000 pazienti e l’83% ha ricevuto raccomandazioni basate sulla genetica, o è stato arruolato in trial clinici, o ha ricevuto nuovi trattamenti; al programma hanno partecipato anche pazienti con malattie rare o in stadio avanzato. Ai pazienti inclusi nel programma, viene eseguito il sequenziamento tumorale e viene raccolta la storia clinica completa. Nel frattempo, il farmacista oncologico rivede la terapia per identificare i prodotti che aumentano il rischio di sanguinamento e che rallentano la guarigione delle ferite. I nuovi trattamenti sono proposti dopo il sequenziamento e dopo un’attenta rivisitazione della letteratura. Settimanalmente il team multidisciplinare si riunisce per discutere dei target genomici e delle possibili terapie che tengano conto dei risultati genetici e delle condizioni del paziente. Per standardizzare le raccomandazioni delle targeted therapies si identificano target selezionati dando priorità alle mutazioni del DNA, alla variazione del numero di copie e alle fusioni di DNA; priorità secondaria è data alle mutazioni trovate con immunoistochimica, mentre la terza priorità è data alla sovraespressione di mRNA da solo.
Dopo la raccolta e l’analisi dei dati clinici del paziente, fa seguito una visita da parte del team multidisciplinare per la discussione dei risultati clinici, delle opzioni terapeutiche o un’eventuale sperimentazione clinica. Infine, i farmacisti discutono col paziente per 30-40 minuti per spiegargli i ritrovamenti genomici, le raccomandazioni sui trattamenti e le informazioni sui trial clinici. È importante quando si parla col paziente usare un linguaggio appropriato in base alle sue conoscenze, adattarlo alla sua comprensione e assicurarsi che abbia compreso; il riassunto di ogni visita col paziente è documentato e riferito all’oncologo, le successive interazioni col paziente legate alle consulenze sui trial clinici e all’approvvigionamento dei farmaci sono condotte dai farmacisti del team.
Il farmacista ha un ruolo fondamentale nell’interpretazione delle sequenze genetiche, nella ricerca dei dati disponibili in letteratura e nel management degli anticoagulanti e delle interazioni delle terapie garantendo la sicurezza del paziente fornendo spiegazioni complete. Si occupa inoltre di procurare i farmaci off label, e della questiona dei rimborsi e dell’assicurazione sanitaria, gestendo l’assistenza al paziente anche nei casi in cui il trattamento non sia coperto da assicurazione, ricercandolo per esempio nei programmi di assistenza farmaceutica delle aziende.
In alcuni tumori solidi i test genetici e la targeted therapy fanno già parte dello standard of care, tuttavia, ci sono ancora molti campi dove la medicina di precisione rappresenta una nuova sfida dove il farmacista può avere un ruolo centrale nella gestione di diversi aspetti delle cure [4].
Bibliografia
- Park JJ, Hsu G, Siden EG, Thorlund K, Mills EJ. An overview of precision oncology basket and umbrella trials for clinicians. Ca can J clin. 2020; 70: 125-137
- National Cancer Institute. Precision Medicine [internet]. [Cited 2021 Nov 6]. Available from: https://www.cancer.gov/publications/dictionaries/cancer-terms/def/precision-medicine
- Oncologia di precisione. Milano. 2018
- Raheem F, Kim P, Grove M, Kiel JP. Precision genomic practice in oncology: pharmacist role and experience in an ambulatory care clinic. Pharmacy (Basel). 2020; 8: 32
- Park JJ, Siden E, Zoratti MJ, Dron L, Harari O, Singer J, et al. Systematic review of basket, umbrella trials and platform trials: a landscape analysis of master protocols. 2019; 20: 572
- Master Protocols: Efficient Clinical Trial Design Strategies To Expedite Development of Oncology Drugs and Biologics. Draft Guidance for Industry. Oct 2018
- Demetri GD, Paz-Ares L, Farago AF, Liu SV, Chawla SP, Tosi D, et al. Efficacy and safety of entrectinib in patients with NTRK fusionpositive (NTRK-fp) Tumors: Pooled analysis of STARTRK-2, STARTRK-1 and ALKA-372-001. Ann of Onc. 2018; Vol 29, suppl 8, VIII713,01
- Hyman DM, Puzanov I, Subbiah V, Faris JE, Chau I, Blay JY, et al. Vemurafenib in Multiple Non melanoma Cancers with BRAF V600 Mutations. N Engl J Med. 2015; 373:726-36.
- Le DT, Durham JN, Smith KN, Wang H, Bartlett BR, Aulakh LK, et al. PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med. 2015; 372(26): 2509–2520
- Redman MW, Papadimitrakopoulou WA, Minichiello K, Hirsch FR, Mack PC, Schwartz LH, et al. Biomarker-driven therapies for previously treated squamous non-small-cell lung cancer (Lung-MAP SWOG S1400): a biomarker-driven master protocol. Lancet Oncol. 2020; Vol 21, Issue 12, P 1589-1601
- Govindan R, Mandrekar SJ, Gerber DE, Oxnard GR, Dahlberg SE, Malik S, et al. ALCHEMIST Trials: A Golden Opportunity to Transform Outcomes in Early Stage Non–Small Cell Lung Cancer. Clin Cancer Res. 2015; 21:5439-5444.
- Schmoll HJ. FOCUS4: a new trial design for evaluation of targeted drugs in colorectal cancer?. Lancet Gastr Hep. 2018; S2468-1253(17)30402-8